Kalkulačka rovnice Arrhenius
Zadajte hodnotu a kliknite na Vypočítajte.Výsledok sa zobrazí .
Čo je kalkulačka Arrheniusovej rovnice?
A kalkulačka rovnice Arrhenius je nástroj, ktorý sa používa na určenie účinku teploty na rýchlosti reakcie v chemických a biologických systémoch. Použije Arrheniusova rovnicu , ktorá vyjadruje vzťah medzi rýchlostnou konštantou (k) reakcie a teplotou (t):
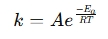
kde:
- k = rýchlostná konštanta (1/s, 1/m · s atď.)
- a = predponponenciálny faktor (frekvencia zrážok)
- ea = aktivačná energia (j/mol)
- r = univerzálna plynová konštanta (8,314 J/mol · k)
- t = absolútna teplota (kelvin)
Preusporiadaná forma sa často používa na porovnanie reakčných rýchlostí pri rôznych teplotách:
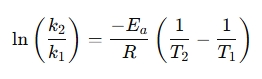
Prečo používať kalkulačku Arrheniusovej rovnice?
- Predpovedá reakčné miery : pomáha chemikom a inžinierom odhadovať, ako rýchlo bude reakcia prebiehať pri rôznych teplotách.
- určuje aktivačnú energiu : Vypočíta energiu potrebnú na to, aby sa vyskytla reakcia.
- V priemyselnej chémii je nevyhnutné
- podporuje environmentálne štúdie : hodnotí teplotné účinky na biologické a atmosférické reakcie.
Ako funguje kalkulačka rovnice Arrhenius?
-
vyžaduje sa vstup :
- Activation Energy (EA) v J/mol
- Teplota (S) v Kelvin (T1, T2)
- Predbodonenciálny faktor (a) (voliteľné)
- rýchlosť konštanty pri jednej teplote (K1) (voliteľné)
-
spracovanie :
- Vypočíta rýchlosť konštmravec (k) pomocou Arrheniusovej rovnice.
- Alternatívne vypočíta aktivačnú energiu (EA) zo známych rýchlostných konštánt.
- používa logaritmické transformácie pre porovnávacie výpočty.
-
výstup :
- Reakčná rýchlostná konštanta (k) pri danej teplote.
- Activation Energy (EA), ak sa na ňu vyrieši.
- Zmena rýchlosti reakcie s teplotou.
Kedy použiť kalkulačku Arrheniusovej rovnice?
- V chémii a kinetike : Pochopenie, ako teplota ovplyvňuje rýchlosti reakcie.
- Vo farmaceutickom vývoji : Štúdium stability liekov a miery degradácie.
- Pri kontrole priemyselného procesu : navrhovanie chemických reakcií citlivých na teplotu.
- V environmentálnej vede : Predpovedanie reakčných miery v klimatických štúdiách a namosférická chémia.
Pomohla vám táto kalkulačka?
Ďakujem za spätnú väzbu


Hľadať kalkulačku
Preskúmajte tisíce bezplatných kalkulačiek, ktorým dôverujú milióny ľudí na celom svete.