Calculadora de equações de Arrhenius
Digite o valor e clique em Calcular.Resultado será exibido .
O que é uma calculadora de equação de Arrhenius?
Uma calculadora de equações Arrhenius é uma ferramenta usada para determinar o efeito da temperatura nas taxas de reação em sistemas químicos e biológicos. Aplica a equação Arrhenius , que expressa a relação entre a taxa constante (k) de uma reação e temperatura (t):
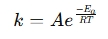
Onde:
- k = taxa constante (1/s, 1/m · s, etc.)
- a = fator pré-exponencial (frequência de colisões)
- ea = energia de ativação (j/mol)
- r = constante de gás universal (8,314 j/mol · k)
- t = temperatura absoluta (Kelvin)
Uma forma reorganizada é frequentemente usada para comparar taxas de reação em diferentes temperaturas:
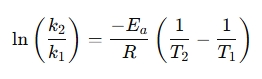
Por que usar uma calculadora de equações de Arrhenius?
- prevê taxas de reação : ajuda químicos e engenheiros a estimar a rapidez com que uma reação prosseguirá em diferentes temperaturas.
- determina a energia de ativação : calcula a energia necessária para que uma reação ocorra.
- essencial na química industrial : Usado em produtos farmacêuticos, ciência de polímeros e engenharia de materiais.
- apóia estudos ambientais : avalia os efeitos da temperatura nas reações biológicas e atmosféricas.
Como funciona uma calculadora de equação de Arrhenius?
-
Entrada necessária :
- Energia de ativação (EA) em J/mol
- Temperatura (s) em Kelvin (T1, T2)
- Fator pré-exponencial (a) (opcional)
- Taxa constante em uma temperatura (K1) (opcional)
-
processamento :
- calcula a taxa constform (k) usando a equação de Arrhenius.
- Alternativamente, calcula a energia de ativação (EA) a partir de constantes de taxa conhecidas.
- Usa transformações logarítmicas para cálculos comparativos.
-
saída :
- Taxa de reação constante (k) a uma determinada temperatura.
- Energia de ativação (EA) se resolver.
- Mudança na taxa de reação com a temperatura.
Quando usar uma calculadora de equações de Arrhenius?
- em química e cinética : entender como a temperatura influencia as velocidades de reação.
- no desenvolvimento farmacêutico : estudando taxas de estabilidade e degradação de medicamentos.
- no controle do processo industrial : projetar reações químicas sensíveis à temperatura.
- na ciência ambiental : prever taxas de reação em estudos climáticos e emQuímica da Mosférica.
Esta calculadora ajudou você?
Obrigado pelo feedback


Calculadora de pesquisa
Explore milhares de calculadoras gratuitas confiáveis por milhões de pessoas no mundo todo.