Arrhenius kalkulator jednadžbe
Unesite vrijednost i kliknite na Izračunavanje.Rezultat će biti prikazan .
Što je Arrheniusov kalkulator jednadžbe?
kalkulator jednadžbe Arrhenius je alat koji se koristi za određivanje učinka temperature na brzinu reakcija u kemijskim i biološkim sustavima. Primjenjuje arrheniusovu jednadžbu , koja izražava odnos između konstante brzine (k) reakcije i temperature (t):
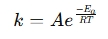
gdje:
- K = konstanta stope (1/s, 1/m · s itd.)
- A = pred-eksponencijalni faktor (učestalost sudara)
- EA = Aktivacijska energija (j/mol)
- r = Univerzalna konstanta plina (8,314 J/mol · K)
- T = Apsolutna temperatura (Kelvin)
Preuređeni oblik često se koristi za usporedbu brzine reakcija na različitim temperaturama:
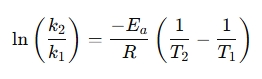
Zašto koristiti Arrhenius kalkulator jednadžbe?
- predviđa stope reakcije : pomaže kemičarima i inženjerima da procijene koliko će brzo reakcija nastaviti na različitim temperaturama.
- određuje aktivacijsku energiju : Izračunava energiju potrebnu za reakciju.
- bitno u industrijskoj kemiji : koristi se u lijekovima, polimernim znanosti i inženjerstvu materijala.
- podržava studije okoliša : Procjenjuje temperaturne učinke na biološke i atmosferske reakcije.
Kako funkcionira Arrheniusov kalkulator jednadžbe?
-
Potreban ulaz :
- Energija aktivacije (EA) u J/Mol
- Temperatura (i) u Kelvinu (T1, T2)
- Pred-eksponencijalni faktor (a) (neobavezno)
- Konstantna brzina na jednoj temperaturi (K1) (opcionalno)
-
obrada :
- Izračunava stopu constmrav (k) Korištenje jednadžbe Arrhenius.
- Alternativno, izračunava aktivacijsku energiju (EA) iz poznatih konstanta brzine.
- Koristi logaritamske transformacije za komparativne proračune.
-
izlaz :
- Konstanta brzine reakcije (k) na određenoj temperaturi.
- Energija aktivacije (EA) ako se rješava za nju.
- Promjena brzine reakcije s temperaturom.
Kada koristiti Arrhenius kalkulator jednadžbe?
- U kemiji i kinetici : Razumijevanje kako temperatura utječe na brzine reakcije.
- U farmaceutskom razvoju : proučavanje stabilnosti lijekova i stope razgradnje.
- U industrijskom kontroli procesa : Dizajniranje kemijskih reakcija osjetljivih na temperaturu.
- u znanosti o okolišu : Predviđanje stope reakcije u klimatskim studijama i ATkemija mosfere.
Je li vam ovaj kalkulator pomogao?
Hvala na povratnim informacijama


Pretraži kalkulator
Istražite tisuće besplatnih kalkulatora kojima vjeruju milijuni diljem svijeta.